Te explicamos qué son las mezclas y cuáles son sus características generales. Además, los tipos de mezclas que existen y ejemplos.

¿Qué son las mezclas?
Se habla de mezcla cuando se combinan dos o más sustancias sin unirse mediante enlaces químicos. En la vida cotidiana las mezclas nos rodean, por ejemplo, muchos fluidos biológicos, como la sangre, son mezclas desde el punto de vista químico.
Puede servirte: Coloides
Métodos de separación de mezclas
Una mezcla puede ser definida como tal solo cuando se pueden volver a obtener las sustancias individuales aplicando procedimientos físicos de separación. Si la mezcla genera algún tipo de reacción química, entonces no se pueden utilizar mecanismos físicos de separación. Los métodos físicos de separación de mezclas más utilizados son la filtración, la decantación y la destilación.
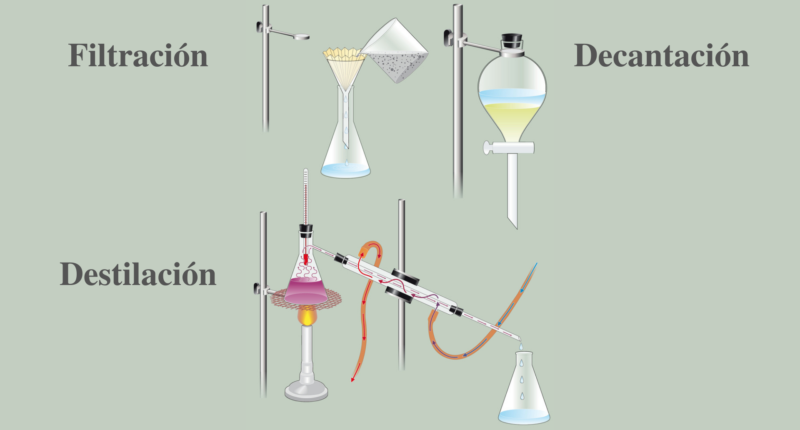
- Filtración. Se emplea para separar pequeñas partículas de sólidos suspendidas en líquidos. Para separar los componentes se utiliza un sistema poroso, por ejemplo un tamiz, así las partículas sólidas más grandes que los agujeros del tamiz quedan atrapadas en él, mientras que el líquido fluye a través de los agujeros.
- Decantación. Se emplea para separar sólidos suspendidos en líquidos y también líquidos inmiscibles (que no se disuelven uno en el otro). La separación se basa en la diferencia de densidades de los componentes de la mezcla. Por lo general, se utiliza un embudo de decantación.
- Destilación. Se emplea para separar mezclas de líquidos. La separación se logra por diferencias en los puntos de ebullición: el líquido que tiene menor punto de ebullición pasa a la fase vapor, luego es condensado (empleando condensadores) y después es juntado en otro recipiente. El líquido que tiene mayor punto de ebullición queda en el recipiente original donde estaba la mezcla.
Más en: Separación de mezclas
Características de las mezclas

- Sus componentes se pueden separar. Las mezclas se generan por la combinación de sustancias bajo ciertas condiciones (calor, presión, etc.). Por eso, también se pueden separar en sus componentes individuales y recuperarlos aplicando procedimientos físicos de separación, como la filtración o la centrifugación (método de separación de sólidos mezclados con líquidos que utiliza la fuerza giratoria).
- Poseen composiciones variables. Esto es especialmente válido en el caso de las mezclas que se presentan en la naturaleza, como el aire, el suelo o el agua de mar, que puede en un determinado momento tener mayor concentración de sales, de nitrógeno, de sólidos en suspensión, etc.
- No forman enlaces químicos. Debe quedar en claro que una mezcla no es una sustancia química, lo que quiere decir que no se origina a consecuencia de reacciones químicas. Es por ello que no hay cambio energético neto en el proceso de mezcla, aunque en algunas disoluciones se produce liberación de calor, que puede llegar a ser muy intensa (como cuando se trata de hacer una solución de ácido sulfúrico o de hidróxido de sodio).
- Pueden ser radiactivas. Algunas mezclas pueden resultar reactivas bajo ciertas condiciones. Por ejemplo, en un motor de combustión interna, la nafta o el gasoil se mezclan con el aire y eso inicia la ignición del motor.
- No tienen fórmula química. No se pueden representar mediante una fórmula química. Al no estar compuestas por proporciones definidas de los elementos que la integran, las mezclas no se pueden expresar mediante una fórmula, como sí sucede con las sustancias de composición conocida.
- Pueden tener una o más fases. En muchas mezclas existen al menos dos fases que se pueden distinguir entre sí, a una se la llama fase dispersa y a la otra, fase dispersante. La dispersante es la fase predominante en el seno de la cual se ubica la fase dispersa. Por otra parte, algunas mezclas, como las disoluciones, tienen una sola fase.
- Algunas propiedades físico-químicas de la fase dispersante pueden variar. Las sustancias que integran la mezcla conservan su naturaleza química, pero algunas propiedades físico-químicas de la fase dispersante pueden variar a causa de la presencia de la fase dispersa. Por ejemplo, el punto de ebullición del agua aumenta y su punto de congelación disminuye al agregar un soluto. Este fenómeno se conoce como “descenso crioscópico” y es importante tenerlo en cuenta en la fabricación de diversos productos.
Tipos de mezclas

Los dos principales tipos de mezclas son:
- Mezclas homogéneas. Sus componentes no se pueden distinguir ni a simple vista ni utilizando lupa o microscopio, ya que se integran de una manera completamente uniforme. Pueden ser líquidas, gaseosas o sólidas, el estado final generalmente depende del disolvente. Las mezclas homogéneas más comunes son las disoluciones de sólidos en líquidos o los sólidos en sólidos, como las aleaciones que se emplean en metalurgia.
- Mezclas heterogéneas. Presentan discontinuidades y a menudo eso se traduce en la formación de fases bien distinguibles a simple vista.
Ejemplos de mezclas
Algunas mezclas homogéneas:
- La lavandina comercial, que puede tener concentraciones variables de hipoclorito de sodio (NaClO).
- Un café con leche
- Una salmuera
- La tintura de yodo
- Algunas aleaciones de metal (acero, aleación de hierro y carbono)
- Azúcar en agua
Algunas mezclas heterogéneas:
- La sangre
- El suelo
- Arena en agua
- Aceite y vinagre
- El cemento
Puede servirte: Estados de agregación
Referencias
- Wikipedia
- Químicas en: https://www.quimicas.net/
- Fisicoquímica, 6ta Edición, Peter William Atkins
¿Te fue útil esta información?
Sí No¡Genial! Muchas gracias por visitarnos :)